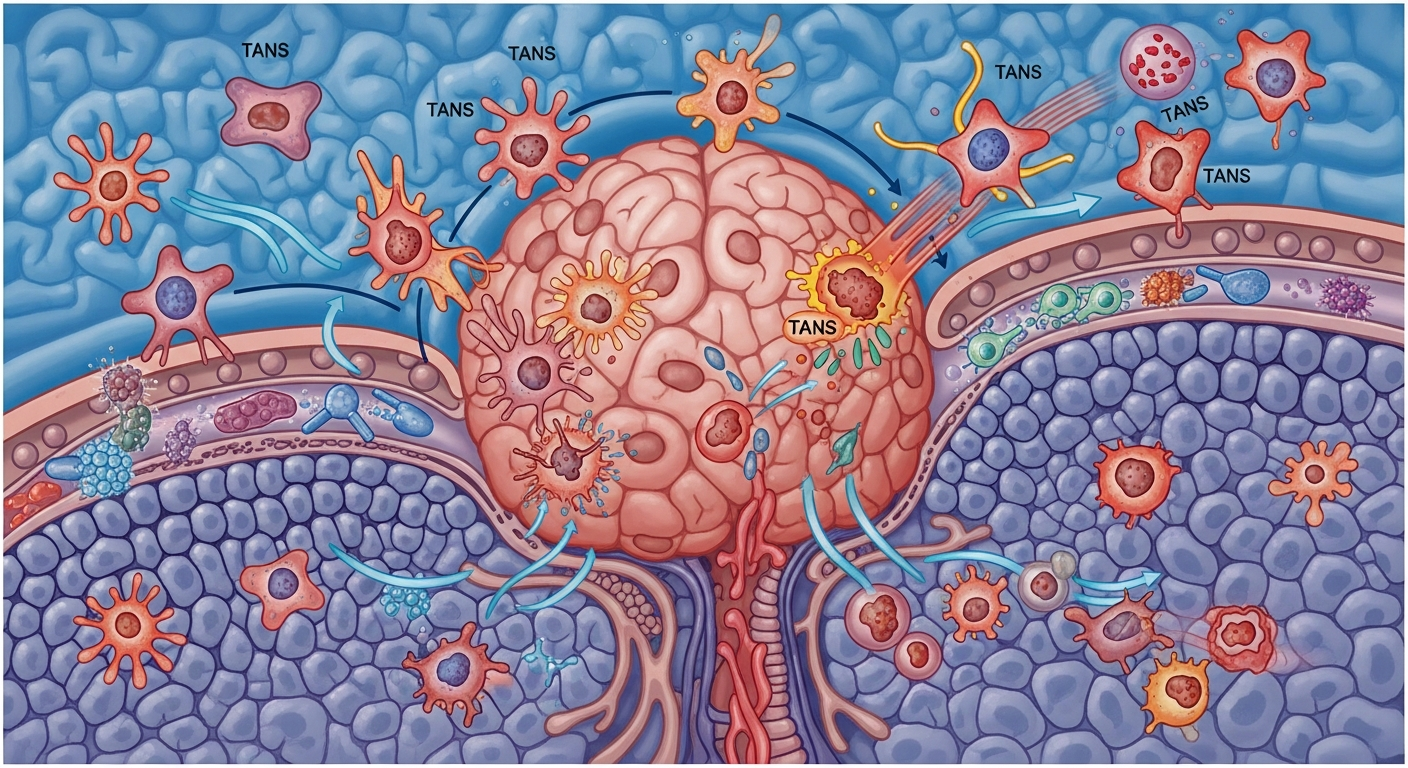
脳腫瘍の微小環境を調節する腫瘍随伴好中球:血液脳関門を通過するナノ粒子の送達
はじめに
悪性度の高い脳腫瘍である膠芽腫(GBM)は、急速な増殖と攻撃的な浸潤を特徴とし、予後不良の原因となります。腫瘍微小環境(TME)における腫瘍随伴好中球(TANs)の役割は複雑であり、N1(抗腫瘍性)とN2(腫瘍促進性)の2つの表現型が存在します。本研究では、数学的モデルを用いて、GBMとTANsの相互作用、および脳の不均一な組織(白質と灰白質)における腫瘍の増殖と浸潤パターンを解析しました。特に、TGF-βやIFN-βといったメディエーターの役割を調査し、治療戦略として、N2 TANsを標的とする抗体療法や、好中球を介したナノ粒子送達による腫瘍細胞の根絶を目指しました。
内容紹介
好中球の動態と腫瘍の増殖
本研究では、GBMとTANsの相互作用をモデル化し、その動態を解析しました。モデルによると、腫瘍細胞から分泌されるTGF-βは、N2 TANsの増殖を促進し、これが腫瘍の成長をさらに促進するという正のフィードバックループを形成することが示されました。逆に、IFN-βはN1 TANsの活性を高め、腫瘍の増殖を抑制しました。これらの結果は、N2 TANsの優位性が腫瘍の予後不良と関連していることを示唆しています。
治療戦略としての抗体療法とナノ粒子送達
N2 TANsを標的とする抗体療法は、N2 TANsの腫瘍促進効果を抑制し、N1 TANsの抗腫瘍効果を強化することで、治療効果を高める可能性が示されました。また、好中球を「トロイの木馬」として利用し、抗がん剤を封入したナノ粒子を腫瘍部位へ送達する戦略も提案されています。このアプローチは、血液脳関門(BBB)や血液腫瘍関門(BTB)を通過する能力を持つ好中球の特性を活用し、標的部位への薬剤送達効率を高めることが期待されます。
手術との併用療法と脳腫瘍の治療
GBMの標準治療である外科的切除後も、残存する浸潤性の腫瘍細胞が再発の原因となります。特に、脳梁(CC)を介した腫瘍細胞の浸潤は、反対側の半球への転移(バタフライGBM)を引き起こし、予後を悪化させます。本研究では、外科的切除と、好中球を介した薬剤送達を組み合わせた併用療法が、腫瘍細胞の浸潤を効果的に制御し、再発を予防できる可能性を示唆しました。このアプローチは、CC周辺組織の切除による認知機能障害などの副作用を軽減しながら、高い抗腫瘍効果をもたらす可能性があります。
考察
腫瘍微小環境における好中球の役割
本研究は、腫瘍微小環境における好中球の二面的な役割、特にN1とN2という異なるフェノタイプが腫瘍の増殖、浸潤、および治療応答にどのように影響するかを数学的モデルを用いて明らかにしました。N2 TANsの優位性が腫瘍の悪性度を高める一方で、N1 TANsは抗腫瘍免疫を促進することが示されました。このN1/N2比率のバランスを制御することが、効果的ながん治療戦略の鍵となるでしょう。
治療戦略の進展と今後の展望
脳腫瘍、特にGBMの治療は、BBBやBTBといった薬剤送達の障壁、および腫瘍細胞の浸潤性により、依然として大きな課題を抱えています。好中球を介したナノ粒子送達システムは、これらの障壁を克服し、標的部位へ薬剤を効率的に届けるための有望なアプローチです。さらに、外科的切除と併用することで、腫瘍の再発や遠隔転移を抑制し、患者のQOL向上に貢献することが期待されます。今後は、ナノ粒子の詳細な動態や、他の免疫細胞との相互作用なども考慮した、より包括的なモデリングと実験的研究が求められます。
脳組織の構造と腫瘍浸潤
脳内の白質と灰白質の構造的違い、特にCCのような神経線維束は、腫瘍細胞の浸潤経路に影響を与えます。モデル解析では、白質組織内での腫瘍細胞の移動が、灰白質よりも速い傾向があることが示されました。また、CCへの浸潤は、バタフライGBMの形成と予後不良に繋がることが示唆されており、この経路を標的とした治療戦略の重要性が浮き彫りになりました。